Применение препаратов гиалуроновой кислоты для лечения остеоартроза
О. В. Оганесян, Л.А. Семенова, А.П. Хапилин, И.С. Косов, В.Г. Салтыкова
Центральный научно-исследовательский институт травматологии и ортопедии им. Н.Н. Приорова, Москва
В отделении ортопедии взрослых ЦИТО проведено лечение 20 больных с посттравматическим остеоартрозом коленного сустава по программе клинических исследований внутрисуставной инъекционной терапии гиалуронанами с применением препарата «Синокром». Для оценки исходного состояния пораженного сустава и эффективности лечения использовались клинический метод, лучевые методы диагностики, морфологическое исследование состояния синовиальной оболочки и суставного хряща, биомеханические методики, а также стандартные опросники и оценочные шкалы. Анализ полученных данных показал безопасность и достаточную эффективность применения «Синокрома» в лечении остеоартроза коленного сустава у пациентов с корригированными травматическими повреждениями. Наибольшая эффективность препарата отмечена на ранних стадиях развития остеоартроза.
Twenty patients with posttraumatic knee osteoarthrosis were treated at the CITO department for adults' orthopedics under the program of clinical study of intraarticular hyaluronic injection therapy using «Synocrom». For the assessment of the affected joint state and treatment efficacy clinical method, radiological diagnosis, morphologic examination of the synovial membrane and articular cartilage, biomechanical methods as well as standard questionnaires and evaluation scales were used. Analysis of the results showed safety and sufficient efficacy of «Synocrom» for the treatment of knee osteoarthrosis in patients after traumatic injury correction. The drug was most effective at the early staged of osteoarthrosis development.
Остеоартроз (деформирующий артроз, остеоартрит — МКБ М15-М19) — хроническое дегенеративно-дистрофическое заболевание суставов, являющееся частой причиной временной и нередко стойкой утраты трудоспособности. По данным эпидемиологических исследований, остеоартрозом различной локализации страдают 1-2% населения до 45 лет и 15_85% людей старшего возраста [3]. Среди всех нозологических форм патологии суставов остеоартроз составляет 55% [8J, а среди ревматических занимает лидирующее место — 60% [4, 5|. Лечение больных деформирующим артрозом является актуальной проблемой травматологии-ортопедии. Необходимость усиленного внимания к этому разделу патологии суставов определяется его высокой социальной значимостью: в последнее десятилетие показатель нетрудоспособности населения в связи с артрозом увеличился до 3 раз [4].
Несмотря на гетерогенность остеоартроза, отмечается однотипность биохимических изменений, приводящих к дальнейшему прогрессированию заболевания со стойким нарушением механической резистивности пораженного сустава и развитием вторичного хронического воспалительного процесса в синовиальной оболочке и параартикулярных тканях [3, 7).
Существующие методы лечения остеоартроза направлены на восстановление баланса между приходящейся на пораженный сустав нагрузкой и его биомеханическими возможностями и включают хирургические воздействия (корригирующие остеотомии, стабилизирующие и реконструктивные операции), общие (снижение массы тела, изменение двигательного режима) и ортопедические реаби-литационно-восстановительные мероприятия (использование специальных брейсов, дополнительных средств опоры, восстановление функции околосуставных мышц). Основные направления медикаментозного лечения остеоартроза — применение нестероидных противовоспалительных препаратов с целью угнетения вторичного воспалительного процесса в синовии, приводящего к дальнейшей деструкции хряща и усугублению клинической симптоматики, и так называемых медленно действующих симптом-модифицирующих препаратов, являющихся компонентами суставного хряща (хондроитин-сульфат, гликозаминогликаны).
Несмотря на широкий спектр имеющихся препаратов и используемых манипуляций, лечение остеоартроза остается сложной задачей, требующей для своего решения комплексного подхода. Зачастую нужный результат не достигается из-за разрозненности и неадекватности проводимых мероприятий и назначений. Действительно, изолированный прием пероральных хондропротекторов, обладающих низкой биодоступностью, как и длительная монотерапия нестероидными противовоспалительными препаратами, редко позволяют добиться ремиссии заболевания и способны вызывать нежелательные побочные эффекты. Кожные аппликации геле-мазевых препаратов также не обеспечивают достаточной концентрации действующего вещества в пораженном суставе из-за низкой биодоступности и требуют частого нанесения (до 4-5 раз в сутки) или применения физиотерапевтических процедур [1).
В этой связи большое значение приобретает включение в комплекс лечебно-реабилитационных мероприятий, направленных на восстановление биохимических и биомеханических характеристик пораженного сустава, патогенетически обоснованной внутрисуставной инъекционной терапии.
Активное изучение уникальных свойств синовиальной жидкости — вязкости (способность поглощать низкочастотные механические нагрузки) и упругости (поглощение и распределение высокочастотных и весовых нагрузок), начатое в 60-е годы прошлого века, позволило установить четкую корреляцию между сохранением механических свойств синовиальной жидкости и концентрацией в ней, а также молекулярной массой гиалуроновой кислоты [6J. Было выявлено, что упругие и вязкостные свойства синовиальной жидкости снижаются у здоровых людей после 25 лет и при остеоартрозе различной локализации за счет нарушения межмолекулярных взаимодействий, уменьшения молекулярной массы и концентрации гиалуронана. Обнаружено также, что гиалуронан синовиальной жидкости проникает в капсулу сустава и связки, обеспечивает их механические свойства, оказывает защитное действие на коллагеновые волокна и клеточные структуры. Это привело к созданию в 1970 г. концепции «вяз-коэластичной поддержки» синовиальных суставов и послужило толчком к производству препаратов гиалуроновой кислоты и дальнейшим исследованиям в данной области [6, 9].
Первые препараты апирогенной гиалуроновой кислоты для офтальмологии с молекулярной массой более 2 МДа были получены в 1968-1970 гг. путем экстракции из биоматериалов. Однако при их применении отмечалось большое число воспалительных реакций, что привело к разработке в 1970 г. высококачественного теста (monkey vitreous test), остающегося до настоящего времени наиболее чувствительным для определения «воспалительной» фракции и хемотаксического агента. Было выявлено присутствие «воспалительной» фракции (IF-NaHA) в полученном гиалуронане, осуществлено ее отделение от «невоспалительной» (NIF-NaHA) и создан эталон препарата гиалуроновой кислоты для применения в медицине. Все современные препараты гиалуроновой кислоты проходят «monkey vitreous test» на наличие антигенной «воспалительной» фракции [9, 10]. В конце 70-х годов 1% NIF-NaHA выпускается под торговыми названиями «Healon» для офтальмологии, «Hyalartil-Vet» для внутрисуставного введения в ветеринарии (Швеция). Проводятся первые клинические испытания: двукратное внутрисуставное введение «Healon» в 200 коленных и 22 тазобедренных суставов при остеоартрозе различной степени выраженности с контрольными группами (введение физиологического раствора или имитация инъекции); срок наблюдения — от 6 до 12 мес. Двойное слепое исследование продемонстрировало статистически достоверное уменьшение болей и повышение повседневной активности пациентов. Вскоре были получены первые препараты гиалуроновой кислоты для внутрисуставных инъекций — «Artz» («Seikagaku and Kaken», Япония, 1987) и «Hyalgan» («Fidia», Италия, 1988), при этом рекомендовано пятикратное их введение с интервалом в одну неделю.
Выполненные многоцентровые исследования позволили выявить уровни действия гиалуронана в синовиальной жидкости — макро-, мини- и микрогомеостаз. Макрогомеосгпаз: при введении гиалуронана в сустав со сниженным в результате синовита содержанием природной гиалуроновой кислоты или с уменьшенной ее молекулярной массой и деградацией вследствие нарушения процессов синтеза -- восстановление вязкоэластичных свойств синовиальной жидкости, стабилизация коллагеновых волокон капсулы и лигаментарного аппарата. Muнuгомеостаз: восстановление скорости транспорта метаболитов от клеток через синовиальную среду в лимфатические сосуды. Отмечается прямая зависимость скорости транссиновиального обмена от механических свойств синовиальной жидкости: при остеоартрозе скорость обмена возрастает в четыре раза, что приводит к нарушению трофических процессов в суставном хряще. Обнаружена возможность поддержания нормального уровня транссиновиального обмена за счет барьерной и механической функции гиалуронана. Микрогомеостаз: восстановление вязкоэластичного окружения клеточных структур синовиальной оболочки, ноцицепторов, угнетение миграции, фагоцитоза и высвобождения простагландинов под действием гиалуронана и стимуляция выроботки собственной гиалуроновой кислоты синовиоцитами А [9].
Современные препараты гиалуроновой кислоты для внутрисуставного введения являются вы-сокоочищеными и производятся по большей части путем биологической ферментации. Молекулярная масса их составляет от 0,9 до 1,6 МДа, за ислючением препарата «Синвиск», являющегося гиланом (гиалуроновая кислота с поперечно «сшитыми» химическим путем молекулами) с молекулярной массой до 6 МДа. Вопрос об оптимальной молекулярной массе гиалуроновой кислоты для внутрисуставного введения остается дискутабельным, данные проведенных многоцентровых исследований противоречивы. По нашим наблюдениям, наилучшее соотношение эффективности внутрисуставной терапии и минимизации побочных явлений имеют препараты со средней молекулярной массой 1-1,6 МДа.
Внутрисуставная инъекционная терапия препаратами гиалуроновой кислоты входит в список мероприятий, рекомендуемых ВОЗ при лечении остеоартроза, с 2003 г. Показанием к внутрисуставному введению гиалуронана является как идиопатический, так и вторичный деформирующий артроз различной локализации, I—III рентгенологической стадии по Kellgren—Lawrence. При наличии выпота в суставе необходимо в первую очередь купировать синовит с помощью медикаментозного лечения, физиотерапевтических процедур, 1-2-кратного введения глюкокортикоидов (дипроспан). Курс инъекционной терапии препаратом гиалуроновой кислоты следует начинать не ранее чем через 2~3 дня после исчезновения внутрисуставного выпота.
Необходимость и возможность повторения курса лечения определяется в процессе клинико-диагностичекого динамического наблюдения пациента.
Противопоказаниями к применению внутрисуставной инъекционной терапии служат индивидуальная непереносимость препарата, наличие внутрисуставного выпота, интраартикулярные инфекции (возможно применение препарата после соответствующей антибиотикотерапии и иммунокор-рекции, при получении трех стерильных посевов синовиальной жидкости в течение не менее 1 мес), инфекции кожных покровов в области предполагаемого введения иглы. Не рекомендуется проводить внутрисуставную инъекционную терапию при системных заболеваниях соединительной ткани в фазе обострения (отсутствие патогенетической обоснованности применения препарата), у детей, беременных и кормящих женщин (отсутствие клинических данных).
В 2005-2006 гг. в отделении ортопедии взрослых ЦИТО проведено лечение 20 больных остео-артрозом коленных суставов по программе клинических исследований внутрисуставной инъекционной терапии гиалуронанами с применением препарата «Синокром» (1% раствор гиалуронана натрия). 1 мл «Синокрома» содержит 10 мг гиалуронана натрия, в состав препарата входят также хлорид натрия, монодигидрогенофосфат натрия, лимонная кислота и вода для инъекций.
В клиническое исследование были включены пациенты в возрасте 18-50 лет, страдающие посттравматическим деформирующим артрозом, перенесшие оперативную или диагностическую артроскопию по поводу повреждения внутрисуставных структур или внутрисуставных переломов коленного сустава, достоверно выявившую посттравматический деформирующий артроз (рис.1, 2), со сроком после операции не менее 2 мес, прошедшие курс первичного реабилитационно-восстановительного лечения. Каждому пациенту было произведено 5 внутрисуставных инъекций «Синокрома» с интервалом в одну неделю.
Оценка начального состояния пораженного сустава и эффективности проведенного лечения включала применение лучевых методов диагностики (рентгенография, УЗИ), морфологическое исследование состояния синовиальной оболочки и суставного хряща (биопсия под контролем ультразвукового датчика), обследование в лаборатории биомеханики (оценка походки, состояния околосуставных мышц) в начале и по завершении курса внутрисуставной инъекционной терапии, использование стандартных опросников и оценочных шкал, в частности шкалы исхода травмы и остеоартроза коленного сустава (Knee Injury and Osteoarthritis Outcome Score — KOOS) [2], перед каждым введением препарата, выявление переносимости последнего.
С учетом актуальности раннего начала лечения посттравматического остеоартроза и высокой чувствительности применяемых методов исследовании в группу были включены пациенты как с рентгенологически манифестированными стадиями (I—II по Kellgren—Lawrence), так и с дорентгенологической стадией заболевания.
Анализ результатов проведенного лечения показал положительную динамику балльной оценки по KOOS у 16 больных: до лечения она составляла от 34 до (57 баллов, после курса лечения повысилась до 82-100 баллов (100 баллов соответствуют отсутствию симптомов), в первую очередь за счет основных подшкал — боль, симптомы и активность повседневной жизни. Сопоставление данных стандартной рентгенографии коленных суставов до и после лечения значимых различий не выявило. При проведении в динамике УЗИ коленных суставов обнаружено уменьшение или купирование признаков хронического воспалительного процесса синовии у 15 пациентов, при этом достоверное увеличение толщины суставного хряща на 0,1 — 1 мм отмечалось лишь у 7 обследуемых (рис. 3). Сравнение результатов гистологического исследования синовиальной оболочки до и после лечения также свидетельствовало об уменьшении или исчезновении хронического воспалительного процесса у 13 больных (рис. 4). Однако нужно отметить «выборочную» информативность данного метода, связанную с необходимостью малоинвазивного выполнения манипуляции и сложностью получения достаточного количества материала.
По данным лаборатории биомеханики, положительная динамика достоверно зафиксирована при помощи инструментальных тестов, оценивающих состояние околосуставных мышц и пассивные и активные движения в коленном суставе, у 18 пациентов, прошедших курс лечения «Синокромом» (рис. 5, 6).
Наибольшая эффективность препарата отмечена при применении его на ранних этапах развития остеоартроза у больных, своевременно получивших необходимое хирургическое лечение. За время проведения клинических исследований ответных реактивных синовитов, общих аллергических реакций и инфекционных осложнений у пациентов не наблюдалось .

Рис. 1. Артроскопическая картина: хондромаляция I—II степени, звездчатый трансхонд-ральный перелом латерального плато большеберцовой кости на фоне застарелого повреждения наружного мениска.
Рис. 2. Артроскопическая картина: хондромаляция I—III степени внутреннего мыщелка бедренной кости, застарелое лоскутное повреждение внутреннего мениска.
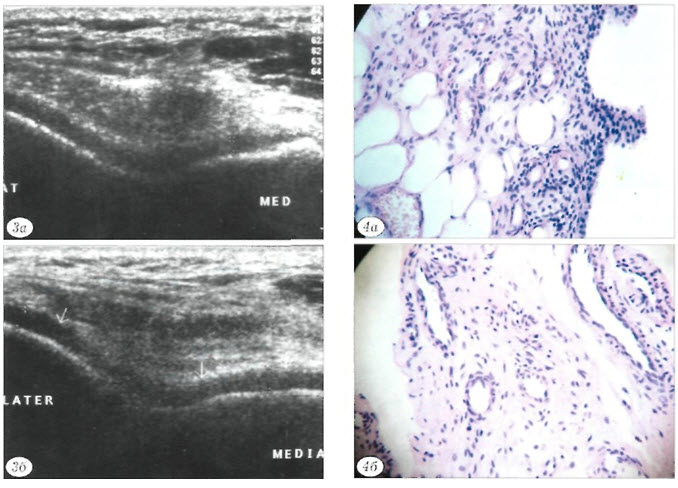
Рис. 3. Ультрасонограммы коленного сустава. a — до курса внутрисуставного применения «Синокрома»: толщина суставного хряща на медиальном мыщелке бедренной кости 1,9-2,3 мм; б — после курса внутрисуставной инъекционной терапии: толщина суставного хряща на медиальном мыщелке бедренной кости 2;5—2,7 мм.
Рис. 4. Гистологические препараты фрагментов синовиальной оболочки коленного сустава. Окраска гематоксилином и эозином, ув. 100. a — до применения «Синокрома»; б — через 2,5 нсд после окончания курса внутрисуставной инъекционной терапии.
Опыт применения «Синокрома» показал безопасность и достаточную эффективность этого препарата в лечении посттравматического остеоартроза коленного сустава у пациентов с корригированными травматическими повреждениями и I—II рентгенологической стадией заболевания по Kellgren—Lawrence. Патогенетическая обоснованность применения «Синокрома», содержащего в качестве активного компонента гиалуроновую кислоту, его гипоаллергенность, отсутствие постинъекционных осложнений позволяют рассматривать внутрисуставную инъекционную терапию этим препаратом как
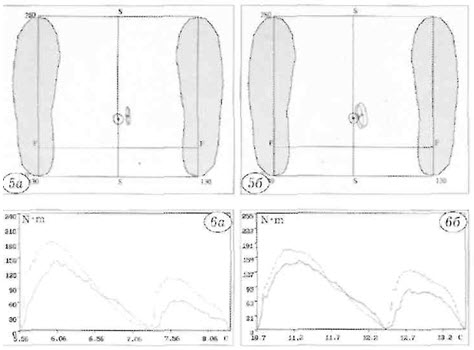
Рис. 5. Данные стабилометрии. a — до применения «Синокрома»: смещение проекции общего центра масс (ОЦМ) вправо на 17,5 мм; б — после курса внутрисуставной инъекционной терапии: нормализация положения проекции ОЦМ, смещение 10 мм.
Рис. 6. Данные изокинетического тестирования околосуставных мышц бедра на аппарате BIODEX (сплошная линия -пораженная, пунктирная линия — здоровая сторона). a — до применения «Синокрома»: снижение работоспособности четырехглавой мышцы бедра на пораженной стороне относительно здоровой до 78%, «гребневидная» форма изокинезиограммы, свидетельствующая о повреждении хряща коленного сустава; б — после курса внутрисуставной инъекционной терапии: повышение работоспособности разгибателей голени до 86%, нормализация формы изокинезиограммы. необходимый элемент лечения пациентов с дегенеративно-дистрофическими заболеваниями суставов.
Литература
1. Беленький А.Г. Локальная инъекционная терапия при дегенеративно-дистрофических заболеваниях опорно-двигательного аппарата: Уч. пособие. — М., 2003. — С. 3-7.
2. Белова А.Н., Щепетова О-Н. Шкалы, тесты и опросники в медицинской реабилитации. — М., 2002. -С. 411-418.
3. Денисов-Никольский Ю.И., Миронов СП., Омельяненко Н.П., Матвейчук И.В. Актуальные проблемы теоретической и клинической остеоартрологии. — М.. 2005. — С. 302; 306-324.
Лучихина Л.В. Артроз. Ранняя диагностика и патогенетическая терапия. — М., 2001.
Насонова В.А., Астапенко М.Г. Клиническая ревматология. — М., 1989. 6. Павлова В.Н. Синовиальная среда суставов. — М., 1980. — С. 119-121; 152-153.
Паалова В.Н., Копъева Т.Н., Слуцкий Л.И., Павлов Г.Г. Хрящ. — М., 1988. — С. 243-249.
Шапиро К.И. Статистика повреждений и заболеваний коленного сустава. — Л., 1981. — С. 3-6.
9. Balazs E.A., Denlinger J.L. //J. Rheumatol. — 1993. -Vol. 20, N 39. — P. 4-8.
10. Denlinger J.L., Balazs E.A. //Exp. Eye Res. — 1980. -Vol. 31. — P. 81-99.
« к списку статтей